|
|
CURSO DE BIOLOGÍAAlejandro Porto Andión |
|
|
|
|
|
|
|
Inicio Temas de Biomoléculas Aula virtual |
|
|
|
|
TEMA 7: GLÚCIDOS.
1.-CONCEPTO Y CLASIFICACIÓN.
Los glúcidos, también llamados azúcares o sacáridos, son un grupo de biomoléculas orgánicas muy abundante en la naturaleza. Concretamente la celulosa, el principal componente de la madera, que es de naturaleza glucídica, quizás sea la biomolécula más abundante en la biosfera. Los glúcidos se definen sencillamente desde el punto de vista químico como polihidroxialdehídos o polihidroxicetonas, o bien sustancias que por hidrólisis dan lugar a este tipo de compuestos. Los polihidroxialdehídos son compuestos orgánicos en los que todos los átomos de carbono están unidos a un grupo hidroxilo excepto uno de ellos que forma parte de un grupo aldehído, mientras que las polihidroxicetonas son compuestos orgánicos en los que todos los átomos de carbono están unidos a un grupo hidroxilo excepto uno que forma parte de un grupo cetona. Muchos glúcidos responden a fórmulas empíricas que se pueden escribir como (C H2O)n, por lo que antiguamente se pensó que eran algún tipo de combinación de carbono y agua y se les llamó hidratos de carbono. Hoy sabemos que esta denominación es químicamente engañosa, pero quizás esté demasiado arraigada como para que sea abandonada definitivamente; de todos modos no se recomienda su uso.
Existen dos clases principales de glúcidos:
a) Monosacáridos.- También llamados osas. Son azúcares simples, no hidrolizables, que consisten en una sola unidad de polihidroxialdehído o polihidroxicetona. Se clasifican a su vez en aldosas y cetosas.
b) Ósidos.- Son azúcares complejos que, cuando sufren hidrólisis, liberan monosacáridos. Están formados por un número variable de monosacáridos unidos covalentemente entre sí. Algunos ósidos se componen exclusivamente de monosacáridos y se denominan holósidos, mientras que otros contienen además otros componentes de naturaleza no glucídica y se denominan heterósidos.
En el siguiente recuadro aparece una clasificación de los distintos tipos de glúcidos.
Algunas de las subdivisiones se irán desarrollando a lo largo de este tema.
2.-MONOSACÁRIDOS.
 Los monosacáridos son los azúcares más sencillos, pues no pueden
descomponerse por hidrólisis para dar lugar a otros azúcares más
simples. En la naturaleza se encuentran en estado libre,
desempeñando importantes funciones, pero también se encuentran
formando parte de otros azúcares más complejos, los ósidos, de los
cuales son sus sillares estructurales.
Los monosacáridos son los azúcares más sencillos, pues no pueden
descomponerse por hidrólisis para dar lugar a otros azúcares más
simples. En la naturaleza se encuentran en estado libre,
desempeñando importantes funciones, pero también se encuentran
formando parte de otros azúcares más complejos, los ósidos, de los
cuales son sus sillares estructurales.
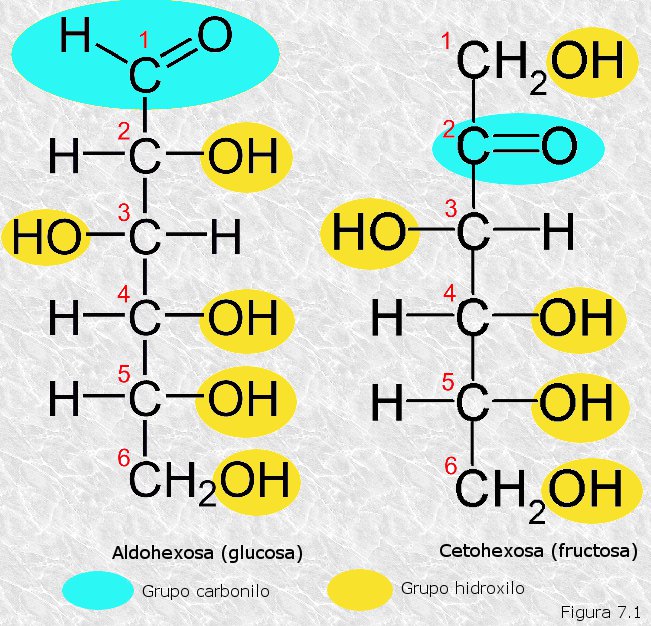
La estructura básica de todos los monosacáridos es una cadena de átomos de carbono no ramificada en la que todos ellos están unidos por enlaces simples. Uno de estos átomos de carbono está unido a uno de oxígeno por un enlace doble formando un grupo carbonilo; todos los demás están unidos a grupos hidroxilo. Si el grupo carbonilo se encuentra en un extremo de la cadena carbonada el monosacárido es un aldehído y recibe el nombre de aldosa; si el grupo carbonilo se encuentra en cualquier otra posición el monosacárido es una cetona y recibe el nombre de cetosa (Figura 7.1). Los monosacáridos naturales tienen entre tres y ocho átomos de carbono, aunque los de siete y ocho son relativamente raros. Según tengan 3, 4, 5, 6... carbonos se denominan respectivamente triosas, tetrosas, pentosas, hexosas.... Existen aldosas y cetosas para cada una de estas longitudes de cadena. La nomenclatura de los monosacáridos se resume en la siguiente tabla:
|
Nº de CARBONOS |
ALDOSAS |
CETOSAS |
|
3 |
ALDOTRIOSAS |
CETOTRIOSAS |
|
4 |
ALDOTETROSAS |
CETOTETROSAS |
|
5 |
ALDOPENTOSAS |
CETOPENTOSAS |
|
6 |
ALDOHEXOSAS |
CETOHEXOSAS |
|
7 |
ALDOHEPTOSAS |
CETOHEPTOSAS |
|
8 |
ALDOOCTOSAS |
CETOOCTOSAS |
Los monosacáridos son compuestos sólidos, cristalinos, de color blanco, solubles en agua y de característico sabor dulce. Entre sus propiedades químicas destaca su poder para reducir el licor de Fehling, siendo esta reacción de gran utilidad para identificarlos experimentalmente.
3.-ESTEREOISOMERÍA DE LOS MONOSACÁRIDOS.
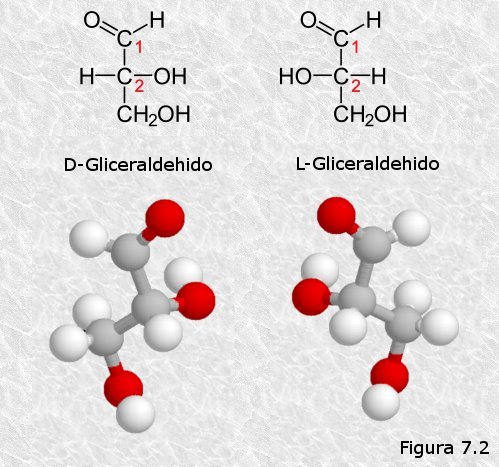
Todos los monosacáridos con excepción de la dihidroxiacetona (una cetotriosa) son compuestos quirales, es decir, poseen uno o más átomos de carbono asimétricos (unidos a 4 sustituyentes distintos), y por lo tanto pueden aparecer en diferentes formas estereoisómeras ópticamente activas. La aldosa más simple, el gliceraldehído, tiene un átomo de carbono asimétrico, y presenta por lo tanto dos formas estereoisómeras que son imágenes especulares no superponibles una de la otra, es decir, dos enantiómeros (Figura 7.2). Para representar sobre el papel las estructuras tridimensionales de los monosacáridos se suelen emplear las llamadas fórmulas en proyección de Fisher tales como las que aparecen en la parte superior de la Figura 7.2. Por convenio se establece que el estereoisómero que, en la proyección de Fisher, presenta el grupo hidroxilo unido al átomo de carbono asimétrico hacia la derecha es el D-gliceraldehído, y el que lo presenta hacia la izquierda es el L-gliceraldehído.
Los monosacáridos de mayor longitud tienen más de un átomo de carbono asimétrico, y por lo tanto aparecen en un número mayor de formas estereoisómeras. En general, un monosacárido con n átomos de carbono asimétricos presenta 2n estereoisómeros. En las aldosas todos los átomos de carbono son asimétricos con excepción del carbono carbonílico y del que se encuentra en el otro extremo de la cadena. Las cetosas, por tener el grupo carbonilo en un carbono secundario, tienen un átomo de carbono asimétrico menos que las aldosas de igual longitud, y por lo tanto tendrán la mitad de estereoisómeros. Una aldosa con x átomos de carbono tendrá n=x-2 carbonos asimétricos; una cetosa tendrá n=x-3. Todo ello aparece resumido en la siguiente tabla.
|
|
nºde carbonos x |
nº de Casimétricos n |
nº de estereoi-sómeros N=2n
|
|
ALDOSAS |
3 |
1 |
21=2
|
|
4 |
2 |
22=4
|
|
|
5 |
3 |
23=8
|
|
|
6 |
4 |
24=16
|
|
|
CETOSAS |
3 |
0 |
20=1
|
|
4 |
1 |
21=2
|
|
|
5 |
2 |
22=4
|
|
|
6 |
3 |
23=8
|
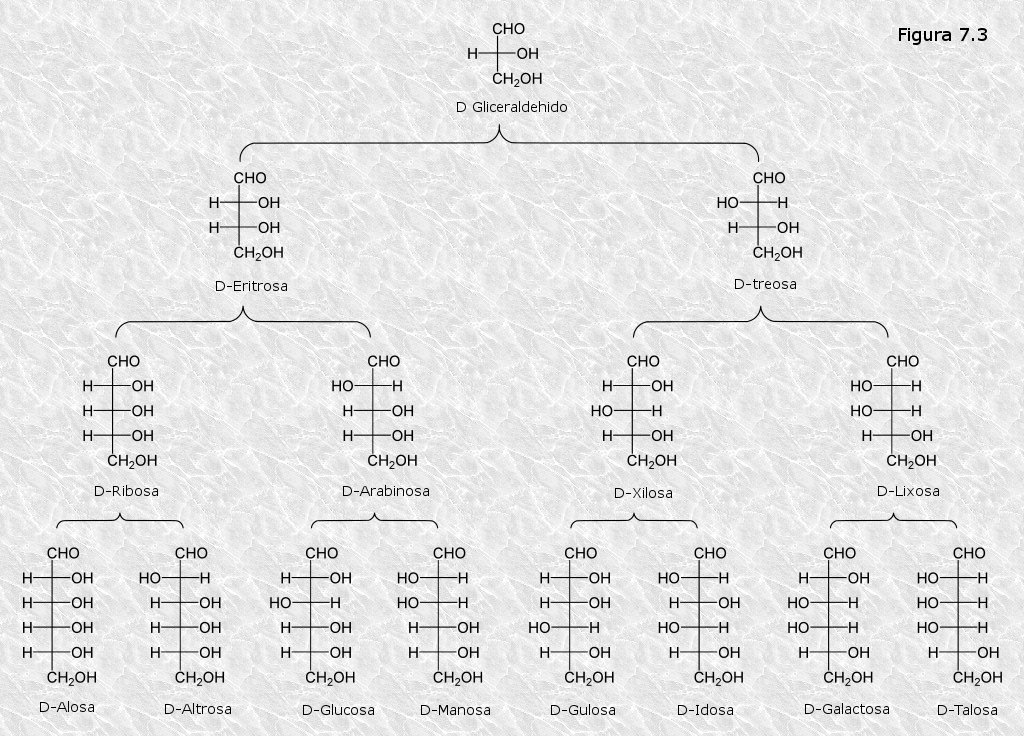
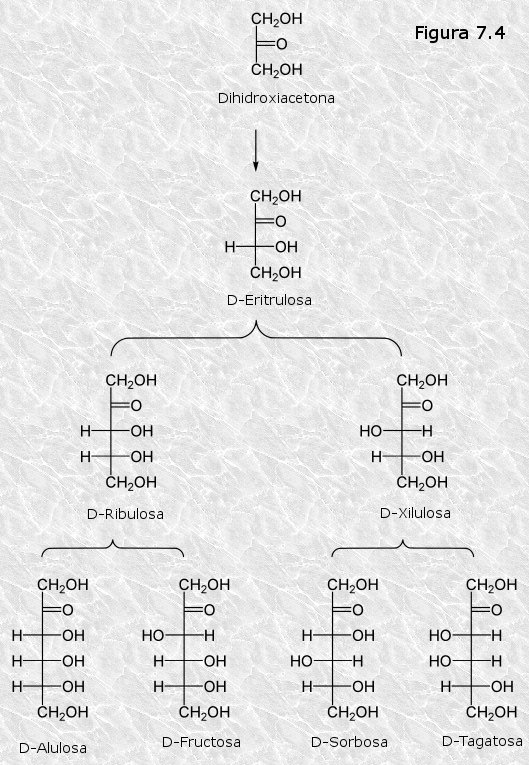
Los estereoisómeros de los monosacáridos de cada una de las diferentes longitudes de cadena se pueden dividir en dos grupos o series atendiendo a la configuración (D o L) del átomo de carbono asimétrico más alejado del átomo de carbono carbonílico. Si ésta es como la del D-gliceraldehído (grupo OH hacia la derecha) el monosacárido pertenece a la serie D; si es como la del L-gliceraldehído pertenece a la serie L. Con muy pocas excepciones, los monosacáridos presentes en la naturaleza pertenecen a la serie D. En la Figura 7.3 se representan las fórmulas estructurales en proyección de Fisher de las aldosas y cetosas de la serie D que tienen entre 3 y 6 átomos de carbono.
Para cada longitud de cadena existen otras tantas formas estereoisómeras pertenecientes a la serie L. Por ejemplo, las aldohexosas poseen 4 átomos de carbono asimétricos, por lo tanto podrán aparecer en 24 = 16 formas estereoisómeras: las ocho que aparecen en la Figura 7.3 y otras ocho pertenecientes a la serie L. Cada uno de los estereoisómeros de la serie D es además enantiómero (imagen especular no superponible) de su homónimo de la serie L (la D-glucosa y la L-glucosa son enantiómeros). Cuando dos estereoisómeros difieren solamente en la configuración de uno de sus átomos de carbono asimétricos se dice que son epímeros (por ejemplo la D-glucosa y la D-manosa)
Por el hecho de poseer centros quirales, los monosacáridos presentan actividad óptica, es decir, cuando se encuentran en disolución acuosa hacen girar el plano de vibración de la luz polarizada. Los monosacáridos que lo hacen girar hacia la derecha se denominan dextrógiros (+) y los que lo hacen girar hacia la izquierda se denominan levógiros (-). El hecho de que un monosacárido sea dextrógiro o levógiro es completamente independiente de su pertenencia a la serie D o a la serie L.
4.-FORMAS ANOMÉRICAS DE LOS MONOSACÁRIDOS.
Cuando se estudiaron las propiedades físicas y químicas de los monosacáridos se pudo comprobar que algunos de ellos, particularmente la glucosa (una aldohexosa), exhibían algunas propiedades anómalas que no cabía esperar de compuestos que presentan las fórmulas estructurales representadas en los cuadros precedentes. En concreto, se observó que el grupo aldehído de la glucosa se comportaba de manera relativamente estable frente a sustancias con las que habitualmente reaccionan con los aldehídos; esto sugiere que el grupo aldehído de la glucosa se encuentra "enmascarado" en su estructura molecular de manera que resulta inaccesible a dichos reactivos. Por otra parte, se observó que las disoluciones de D-glucosa exhibían un extraño comportamiento en relación con su rotación óptica característica. La rotación óptica es el ángulo que gira el plano de vibración de la luz polarizada al atravesar una disolución de una sustancia ópticamente activa. Cuando se medía la rotación óptica de diferentes disoluciones de D-glucosa se comprobó con sorpresa que en unos casos ésta tenía un valor inicial de +112,2º mientras que en otros este valor era de +18,7º. Resultaba sin embargo todavía más sorprendente que al cabo de unos minutos de haber preparado la disolución la rotación óptica cambiaba para estabilizarse en todos los casos en un valor de +52,7º. Este cambio en la rotación óptica se denomina mutarrotación. El fenómeno de la mutarrotación sugiere que deben existir dos formas estereoisómeras de la D-glucosa con propiedades físicas diferentes.
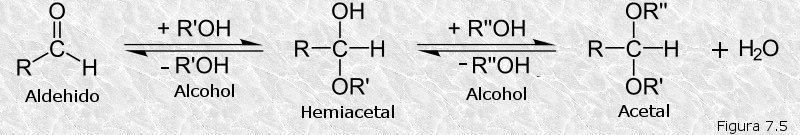
La causa de que la D-glucosa (y también otros monosacáridos) exhiba estas anómalas propiedades reside en que este azúcar no se encuentra habitualmente en disolución en la forma de cadena abierta, tal y como se representa mediante la proyección de Fisher, sino en una forma cíclica denominada anillo de piranosa. Los aldehídos y las cetonas en general reaccionan con los alcoholes para formar unos compuestos llamados respectivamente hemiacetales y hemicetales (Figura 7.6), que poseen un átomo de carbono asimétrico adicional y pueden por lo tanto existir en dos formas estereoisómeras . Un caso particular de este tipo de reacción se da en la D-glucosa cuando el grupo aldehído del átomo de carbono 1 reacciona con el grupo hidroxilo del átomo de carbono 5 para formar un hemiacetal intramolecular de forma cíclica que, por analogía con el compuesto con el compuesto heterocíclico de seis átomos denominado pirano, recibe el nombre de anillo de piranosa. Tal reacción intramolecular se representa en la siguiente animación.
Como consecuencia de esta reacción intramolecular, el átomo de carbono carbonílico de la D-glucosa, que no era asimétrico en la forma de cadena abierta, se transforma en un átomo de carbono asimétrico. Por ello, la D-glucosa puede existir en dos formas estereoisómeras denominadas respectivamente α-D-glucosa y β-D-glucosa (ver Figura 7.6). Este tipo particular de estereoisómeros reciben el nombre de anómeros o formas anoméricas y el átomo de carbono carbonílico, responsable de su aparición, el de carbono anomérico.
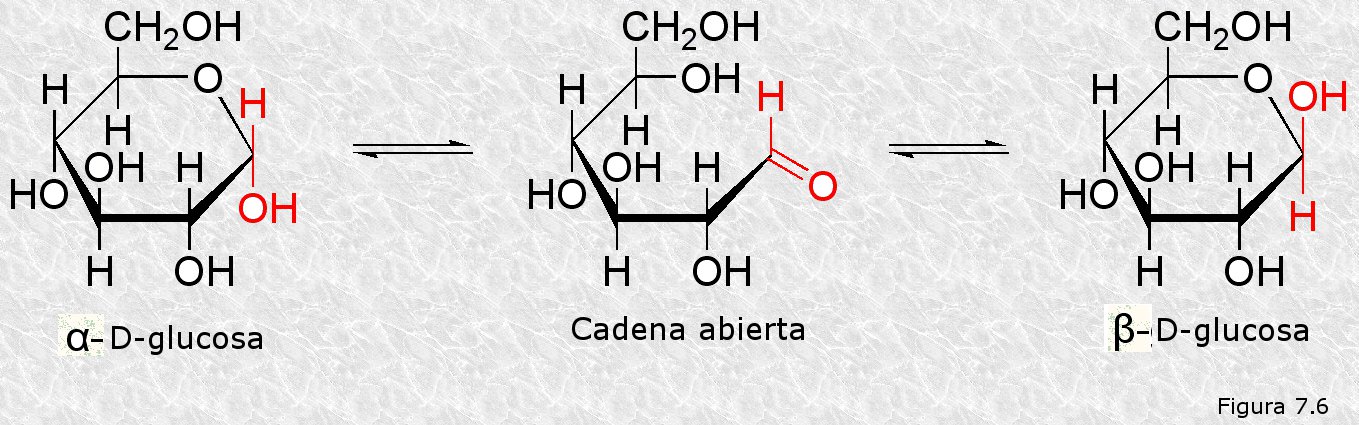
La existencia de estas dos formas anoméricas de la glucosa explica sus propiedades anómalas. En primer lugar, es lógico que no reaccione como lo hacen los aldehídos, ya que su grupo carbonilo no existe en realidad como tal, sino que ha reaccionado previamente para formar el hemiacetal intramolecular. En segundo lugar, el fenómeno de la mutarrotación adquiere sentido si consideramos que existen dos estereoisómeros (α y β) cada uno de los cuales exhibirá en disolución una rotación óptica característica. Estas dos formas anoméricas son interconvertibles a través de la forma de cadena abierta. Cuando se prepara una disolución, ya sea de α o de β-D-glucosa, se alcanza al cabo de unos minutos una mezcla de ambas que en el equilibrio estará formada por 2/3 de β-D-glucosa y 1/3 de α-D-glucosa. Esta mezcla en el equilibrio es la que presenta una rotación óptica de +52,7º.
Además de la glucosa, otros muchos monosacáridos pueden dar lugar a hemiacetales o hemicetales intramoleculares. Por ejemplo, la D-fructosa (una cetohexosa) da lugar, por reacción intramolecular entre el grupo cetona del carbono 2 y el grupo hidroxilo del carbono 5, a una forma cíclica diferente, que, por analogía con el compuesto heterocíclico de cinco átomos denominado furano, recibe el nombre de anillo de furanosa. Como consecuencia, la D-fructosa presenta dos formas anoméricas: la α-D-fructosa y la β-D-fructosa. La glucosa también puede dar lugar a anillos de furanosa por reacción entre C1 y C4, pero el anillo de piranosa resulta más estable.
Las fórmulas de proyección de Fisher no resultan útiles para representar los monosacáridos en forma cíclica, por lo que habitualmente se utilizan para ello las llamadas fórmulas en perspectiva de Haworth, que son las que se muestran en la Figura 7.6. En estas fórmulas los anillos de piranosa y furanosa se representan como anillos planares con los distintos sustituyentes de los átomos de carbono proyectándose por encima y por debajo del plano del anillo. Los sustituyentes que aparecen a izquierda y derecha de la proyección de Fisher en la fórmula de Haworth aparecen hacia arriba y hacia abajo respectivamente. Los anómeros α se representan con el grupo -OH del carbono anomérico hacia abajo y los anómeros β con dicho grupo -OH hacia arriba.
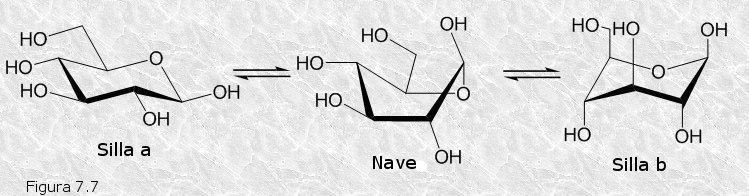
Aunque las fórmulas de Haworth proporcionan una idea bastante próxima a la realidad acerca de las estructuras cíclicas de los monosacáridos, hay que tener en cuenta que en realidad, si bien el anillo de furanosa es casi totalmente planar, el de piranosa, debido a las restricciones que impone la geometría de los orbitales del carbono, tiende a adoptar una de las dos conformaciones representadas en la Figura 7.7, que reciben el nombre de "silla" y "nave". Existen dos tipos de "silla" que se interconvierten a través de la forma "nave".
No todos los monosacáridos pueden dar lugar a hemiacetales o hemicetales intramoleculares. Para que éstos se formen es necesario que los dos grupos funcionales (carbonilo e hidroxilo) que han de reaccionar se acerquen lo suficiente para hacerlo, y esto sólo sucede si la cadena carbonada es lo bastante larga como para que la libre rotación de los enlaces simples permita este acercamiento. Por ello, los monosacáridos de 3 y 4 átomos de carbono se encuentran siempre en forma de cadena abierta, mientras que los de 5 ó más carbonos tienden a formar anillos de piranosa o furanosa en función de cual de ellos sea más estable en cada caso. En la siguiente tabla se muestran las formas más estables en que aparecen los monosacáridos de 3 a 6 átomos de carbono. Obsérvese que las cetosas necesitan una mayor longitud de cadena para poder dar lugar a formas cíclicas; ello se debe a que su átomo de carbono carbonílico no está al final de la cadena como en las aldosas.
|
Nº de C |
ALDOSAS |
CETOSAS |
|
3 |
CADENA ABIERTA |
CADENA ABIERTA |
|
4 |
CADENA ABIERTA |
CADENA ABIERTA |
|
5 |
FURANOSA |
CADENA ABIERTA |
|
6 |
PIRANOSA |
FURANOSA |
5.-DERIVADOS DE LOS MONOSACÁRIDOS.
Además de los monosacáridos simples, existe en la naturaleza una serie de derivados de los mismos que tienen una gran importancia biológica, sobre todo los derivados de algunas aldohexosas como la glucosa, manosa y galactosa. Estos derivados se obtienen por sustitución de alguno de los grupos hidroxilo por algún otro grupo funcional, o bien por oxidación o reducción de alguno de los átomos de carbono del monosacárido original.
Entre ellos cabe destacar los siguientes:
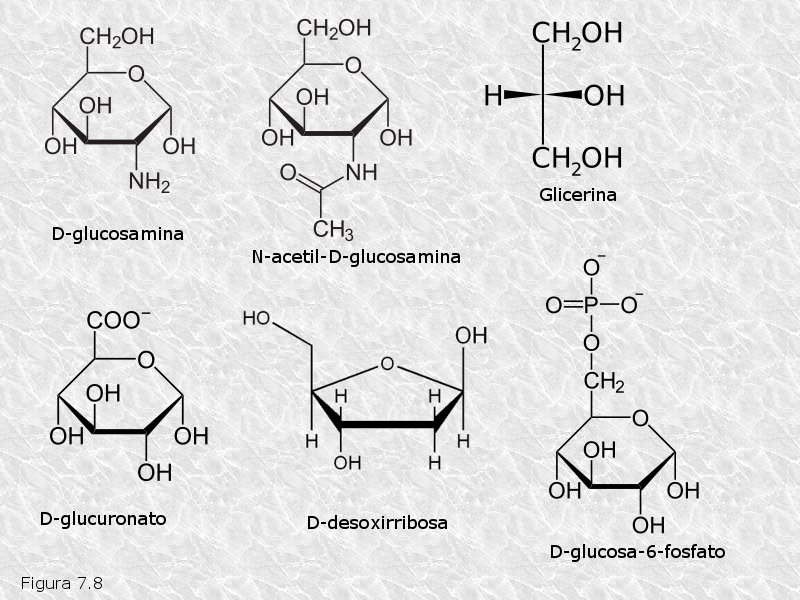
1) Aminoazúcares.- En ellos el grupo hidroxilo unido al carbono 2 del monosacárido de origen está sustituido por un grupo amino. Así sucede por ejemplo en la glucosamina, manosamina y galactosamina, que son los más importantes. En ocasiones este grupo amino aparece acetilado, como en la N-acetil-glucosamina. (Figura 7.8)
2) Azúcares-alcoholes.- Se obtienen por reducción del grupo carbonilo a grupo hidroxilo, de manera que en ellos todos los átomos de carbono están unidos a grupos hidroxilo. Entre los azúcares-alcoholes destaca la glicerina, un polialcohol de tres átomos de carbono que se encuentra formando parte de muchos lípidos.
3) Azúcares-ácidos.- Se obtienen por oxidación de algún átomo de carbono del monosacárido de origen a grupo carboxilo. Si el carbono oxidado es el carbono carbonílico se obtienen los ácidos aldónicos; si es el carbono hidroxílico del otro extremo de la cadena se obtienen los ácidos urónicos (Figura 7.8). Entre los azúcares-ácidos destacan los derivados de la glucosa denominados ácido glucónico (un ácido aldónico) y ácido galacturónico (un ácido urónico). Los azúcares-ácidos se encuentran normalmente ionizados a pH 7, por lo que se pueden nombrar correctamente como gluconato, glucuronato, etc.
4) Desoxiazúcares.- En ellos, alguno de los grupos hidroxilo del monosacárido de origen está sustituido por un átomo de hidrógeno. El más importante es la 2´-desoxirribosa, que forma parte de los ácidos nucleicos.
5) Azúcares-fosfato.- Son azúcares fosforilados (unidos a un grupo fosfato mediante enlace éster) en alguno de sus grupos hidroxilo. En la síntesis y degradación de los glúcidos, los compuestos intermedios no suelen ser los propios azúcares sino sus derivados fosforilados. Ello se debe a que estos derivados poseen cargas netas a pH 7, lo que evita su difusión a través de las membranas celulares.
6) Glucósidos.- Es sabido que los hemiacetales y hemicetales pueden reaccionar con una segunda molécula de alcohol para, liberando una molécula de agua, dar lugar a acetales y cetales respectivamente (Figura 7.5). Un caso particular de este tipo de reacción lo constituye la que se produce entre un monosacárido en forma cíclica (que es un hemiacetal o hemicetal intramolecular) y un alcohol para formar un glucósido liberando una molécula de agua. El interés de este tipo de compuestos reside en que el tipo de enlace mediante el cual se unen los monosacáridos para formar ósidos puede considerarse como un caso particular de la reacción entre un monosacárido y un alcohol para formar un glucósido.
6.-EL ENLACE GLUCOSÍDICO.
Los monosacáridos capaces de formar anillos de piranosa o furanosa, en tanto que hemiacetales o hemicetales intramoleculares, pueden reaccionar con los alcoholes para formar glucósidos liberándose en el proceso una molécula de agua. Un caso particular de este tipo de reacción se da cuando el grupo hidroxilo de la molécula de alcohol es aportado por un segundo monosacárido. El compuesto resultante, un disacárido, estará formado por dos monosacáridos unidos mediante enlace glucosídico. Así pues, el enlace glucosídico resulta de la formación de un acetal (o cetal) entre el carbono carbonílico de un monosacárido y un grupo hidroxilo de otro monosacárido. Este segundo monosacárido posee otro carbono carbonílico libre que a su vez puede reaccionar con un grupo hidroxilo de un tercer monosacárido para formar otro enlace glucosídico, y así sucesivamente. De este modo, mediante sucesivos enlaces glucosídicos, se puede unir un número ilimitado de monosacáridos para formar largas cadenas que pueden ser lineales o ramificadas. En todos los ósidos, azúcares formados por un número variable de monosacáridos unidos entre sí, la unión entre los mismos se realiza mediante este tipo de enlace.
El enlace glucosídico puede ser de dos tipos, α o β, según sea α o β la configuración del monosacárido que aporta al enlace el átomo de carbono carbonílico (Figura 7.9). Por otra parte, se distinguen enlaces glucosídicos monocarbonílicos, en los que sólo está implicado el carbono carbonílico de un monosacárido, y enlaces glucosídicos dicarbonílicos, en los que están implicados los carbonos carbonílicos de los dos monosacáridos enlazados.
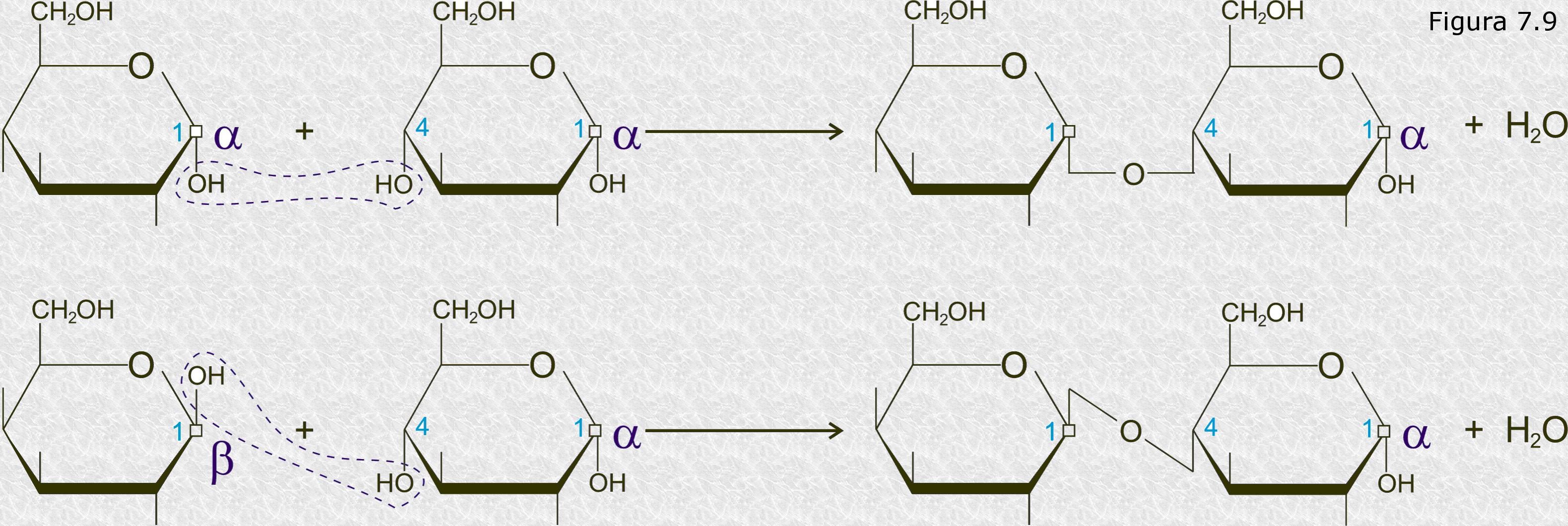
La estructura de un enlace glucosídico se suele especificar escribiendo el tipo de enlace, α o β, seguido entre paréntesis por los números de los átomos de carbono implicados en él; el número que se escribe en primer lugar corresponde al átomo de carbono carbonílico. Algunos ejemplos son α(1—›4), α(1—›6), β(1—›4), β(1—›2), etc. Puesto que los monosacáridos tienen muchos grupos hidroxilo, la variedad de enlaces glucosídicos posibles es enorme; no obstante, los más abundantes en la naturaleza son los α(1—›4) y los β(1—›4).
7.-OLIGOSACÁRIDOS.
Los ósidos, glúcidos formados por la unión de varios monosacáridos, pueden ser holósidos, si están formados exclusivamente por monosacáridos, o heterósidos, si además contienen otros componentes de naturaleza no azucarada. Entre los holósidos se distinguen, en función del número de unidades que los forman, dos tipos: oligosacáridos y polisacáridos.
 Los
oligosacáridos (del griego oligos = poco) son
holósidos compuestos por un número reducido de unidades
monosacarídicas unidas mediante enlaces glucosídicos. El número de
unidades monosacarídicas que forman parte de un oligosacárido puede
oscilar entre 2 y 10. Si están formados por sólo dos
monosacáridos se denominan disacáridos, si lo están por tres
trisacáridos; a los que están formados por más de tres
monosacáridos no se le suele asignar ninguna denominación específica
y se suelen nombrar sencillamente como oligosacáridos. Sus
propiedades físicas son muy similares a las de los monosacáridos:
también son sólidos cristalinos, de color blanco, sabor dulce y
solubles en agua. La mayoría de ellos conserva el poder reductor
característico de los monosacáridos. Este poder reductor reside en
los átomos de carbono carbonílicos y se pierde cuando éstos
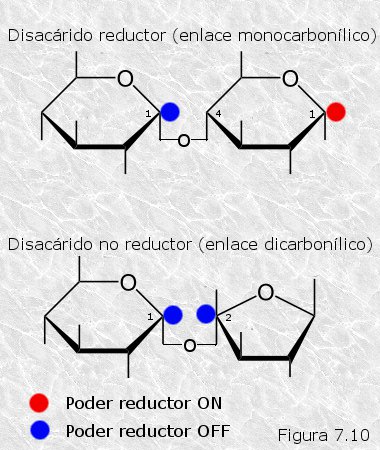
participan en un enlace glucosídico. Por ello, cuando dos
monosacáridos se unen mediante un enlace glucosídico monocarbonílico
el disacárido resultante tendrá poder reductor, ya que conserva un
carbono carbonílico libre. Por el contrario, si el enlace es
dicarbonílico el disacárido resultante, al tener sus dos carbonos
carbonílicos implicados en el enlace, habrá perdido el poder
reductor (Figura
7.10). En general, los oligosacáridos, independientemente de su
longitud, tendrán poder reductor siempre que conserven algún carbono
carbonílico libre en uno de sus extremos, que se denomina extremo
reductor.
Los
oligosacáridos (del griego oligos = poco) son
holósidos compuestos por un número reducido de unidades
monosacarídicas unidas mediante enlaces glucosídicos. El número de
unidades monosacarídicas que forman parte de un oligosacárido puede
oscilar entre 2 y 10. Si están formados por sólo dos
monosacáridos se denominan disacáridos, si lo están por tres
trisacáridos; a los que están formados por más de tres
monosacáridos no se le suele asignar ninguna denominación específica
y se suelen nombrar sencillamente como oligosacáridos. Sus
propiedades físicas son muy similares a las de los monosacáridos:
también son sólidos cristalinos, de color blanco, sabor dulce y
solubles en agua. La mayoría de ellos conserva el poder reductor
característico de los monosacáridos. Este poder reductor reside en
los átomos de carbono carbonílicos y se pierde cuando éstos
participan en un enlace glucosídico. Por ello, cuando dos
monosacáridos se unen mediante un enlace glucosídico monocarbonílico
el disacárido resultante tendrá poder reductor, ya que conserva un
carbono carbonílico libre. Por el contrario, si el enlace es
dicarbonílico el disacárido resultante, al tener sus dos carbonos
carbonílicos implicados en el enlace, habrá perdido el poder
reductor (Figura
7.10). En general, los oligosacáridos, independientemente de su
longitud, tendrán poder reductor siempre que conserven algún carbono
carbonílico libre en uno de sus extremos, que se denomina extremo
reductor.
Los oligosacáridos más abundantes y de mayor importancia biológica son los disacáridos. En la siguiente tabla se muestra la composición de los disacáridos más relevantes.
|
MALTOSA |
Glucosa-α(1—›4)-Glucosa |
|
ISOMALTOSA |
Glucosa-α(1—›6)-Glucosa |
|
CELOBIOSA |
Glucosa-β(1—›4)-Glucosa |
|
LACTOSA |
Galactosa-β(1—›4)-Glucosa |
|
TREHALOSA |
Glucosa-α(1—›1)-Glucosa |
|
SACAROSA |
Fructosa-β(2—›1)-Glucosa |
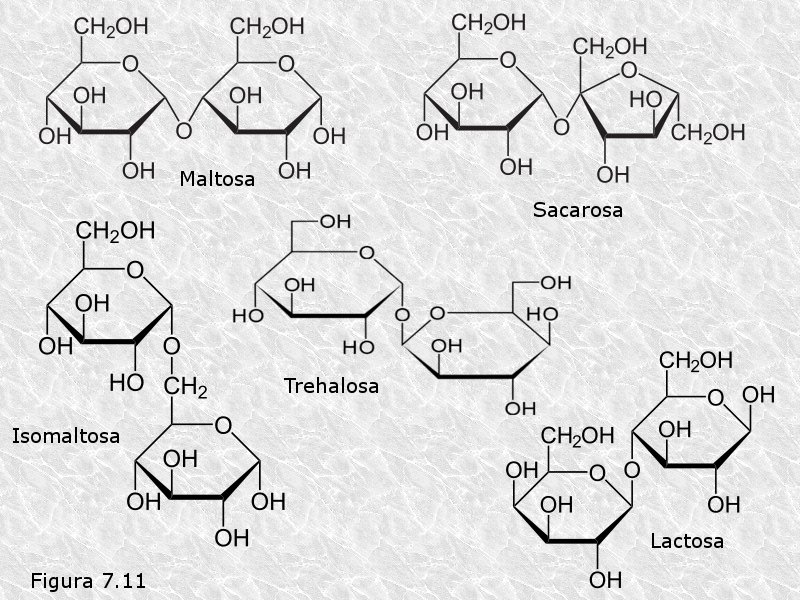
La maltosa (Figura 7.11) y la isomaltosa son dos de los productos de la hidrólisis incompleta del almidón y del glucógeno (dos polisacáridos de reserva) durante la digestión. La celobiosa, que no se encuentra libre en la naturaleza, se obtiene por hidrólisis de la celulosa (un polisacárido estructural). La lactosa (Figura 7.11) se encuentra exclusivamente en la leche de los mamíferos. La trehalosa es el constituyente principal del fluido circulante (hemolinfa) de los insectos. La sacarosa (azúcar de mesa) es un disacárido de especial importancia; se encuentra exclusivamente en el mundo vegetal y es uno de los productos directos de la fotosíntesis que estos realizan, constituyendo la principal forma de transporte de azúcares desde las hojas hacia otras partes de la planta. Obsérvese que maltosa, isomaltosa, celobiosa y lactosa son disacáridos reductores, mientras que trehalosa y sacarosa, por poseer enlaces glucosídicos dicarbonílicos, son no reductores. La sacarosa se puede escribir también como Glucosa-α(1—›2)-Fructosa.
En cuanto a los trisacáridos, relativamente escasos en la naturaleza, cabe citar algunos como la rafinosa y la melicitosa que se encuentran en la savia de determinadas plantas.
Además de los disacáridos y trisacáridos, existe una gran variedad de oligosacáridos naturales con estructuras químicas muy diversas. Se trata de compuestos formados por un número de monosacáridos que oscila entre 4 y 10 unidos entre sí por enlaces glucosídicos dando lugar a cadenas que pueden ser lineales o ramificadas. Normalmente no se encuentran en estado libre, sino unidos covalentemente a otras biomoléculas como lípidos o proteínas. La cara externa de las membranas celulares se halla cuajada de cadenas oligosacarídicas unidas a los lípidos y proteínas de membrana que cumplen importantes funciones en los procesos de reconocimiento de la superficie celular.
8.-POLISACÁRIDOS.
Los polisacáridos son glúcidos formados por un número elevado de monosacáridos unidos entre sí mediante enlaces glucosídicos. En el proceso de unión de n monosacáridos para formar un polisacárido se liberan (n-1) moléculas de agua, una por cada enlace glucosídico. Aunque el límite entre oligosacáridos y polisacáridos se suele fijar arbitrariamente en 10 unidades monosacarídicas constituyentes, lo cierto es que la mayoría de los polisacáridos naturales están formados por centenares o miles de estas unidades monoméricas.
Los polisacáridos son macromoléculas de elevado peso molecular y estructura compleja. Así como otras macromoléculas tienen tamaños y pesos moleculares definidos, en los polisacáridos éstos pueden variar en función del estado metabólico de la célula. Se puede considerar que los monosacáridos son los sillares estructurales de los polisacáridos, al igual que los aminoácidos lo son de las proteínas o los nucleótidos de los ácidos nucleicos. Las propiedades físicas y químicas de los polisacáridos son en cierto modo contrarias a las que exhiben monosacáridos y oligosacáridos: no cristalizan, no tienen sabor dulce, carecen de poder reductor, y, aunque son sustancias hidrofílicas, son poco soluble en agua debido a su elevado peso molecular.
Los distintos tipos de polisacáridos difieren entre sí en el tipo de unidades monosacarídicas que los forman, en el tipo de enlace glucosídico (α o β) que las une, y en el mayor o menor grado de ramificación que presentan sus cadenas. Se distinguen dos tipos principales de polisacáridos, los homopolisacáridos, formados por un sólo tipo de monosacárido, y heteropolisacáridos, formados por dos o más tipos de monosacáridos. Los homopolisacáridos de la D-glucosa, denominados glucanos, son los polisacáridos más abundantes en la naturaleza y los que tienen una mayor importancia biológica. Algunos de ellos desempeñan una función energética, como el almidón y el glucógeno, mientras que otros, como la celulosa, realizan una función de tipo estructural. Hay que destacar que aquéllos que presentan enlaces glucosídicos tipo α tienen función energética, mientras que los que los presentan tipo β tienen función estructural. A continuación analizaremos la estructura y la función de los tres glucanos más importantes: el almidón, el glucógeno y la celulosa.
A) Almidón.- Es un polisacárido formado por moléculas de α-D-glucosa unidas por enlaces glucosídicos α(1—› 4) y α(1—›6). En la molécula de almidón se distinguen dos tipos de polímero:
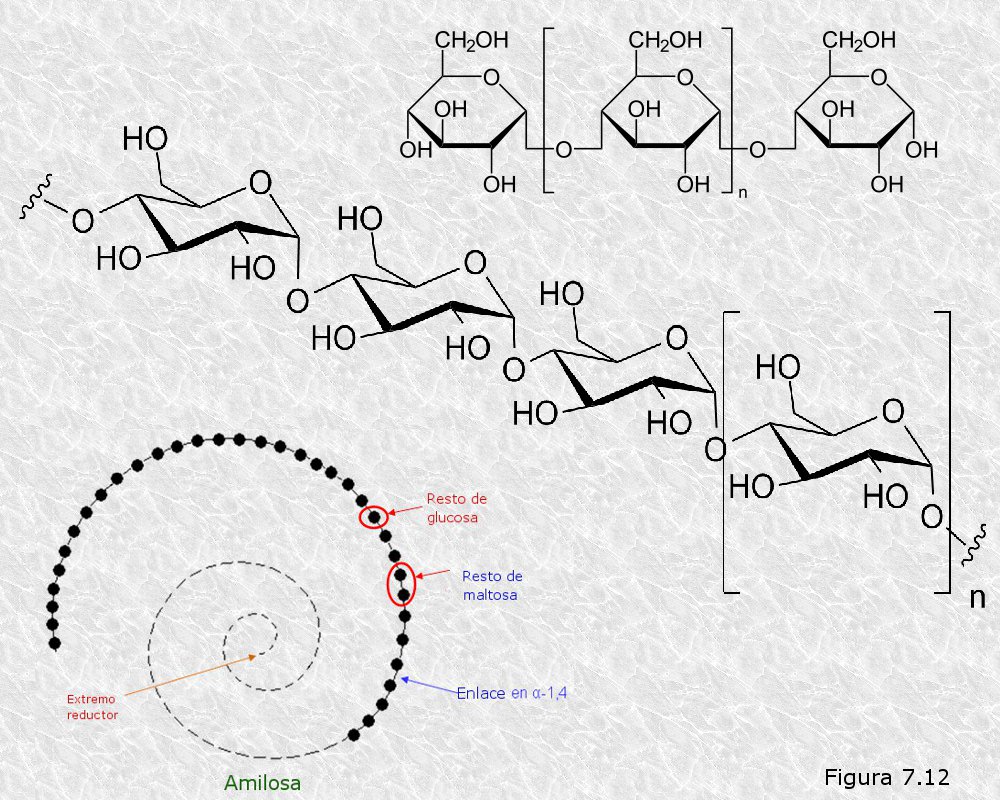
Amilosa.- Es un polímero no ramificado formado por largas cadenas por varios centenares de unidades de α-D-glucosa unidas por enlaces α-(1—›4). Estas cadenas adoptan una disposición helicoidal con 6 moléculas por vuelta, y tienen masas moleculares relativas que oscilan entre unos pocos miles y 500.000 daltons (Figura 7.12).
Amilopectina.- Es un polímero muy ramificado (Figura 7.13) formado por moléculas de α-D-glucosa. Los sucesivos restos de glucosa a lo largo de las cadenas están unidos por enlaces α(1—›4), y los puntos de ramificación, que se encuentran espaciados por un número de restos de glucosa que oscila entre 24 y 30, consisten en enlaces α(1—›6) (ver Figura 7.13). Su masa molecular relativa puede alcanzar hasta un millón de daltons.
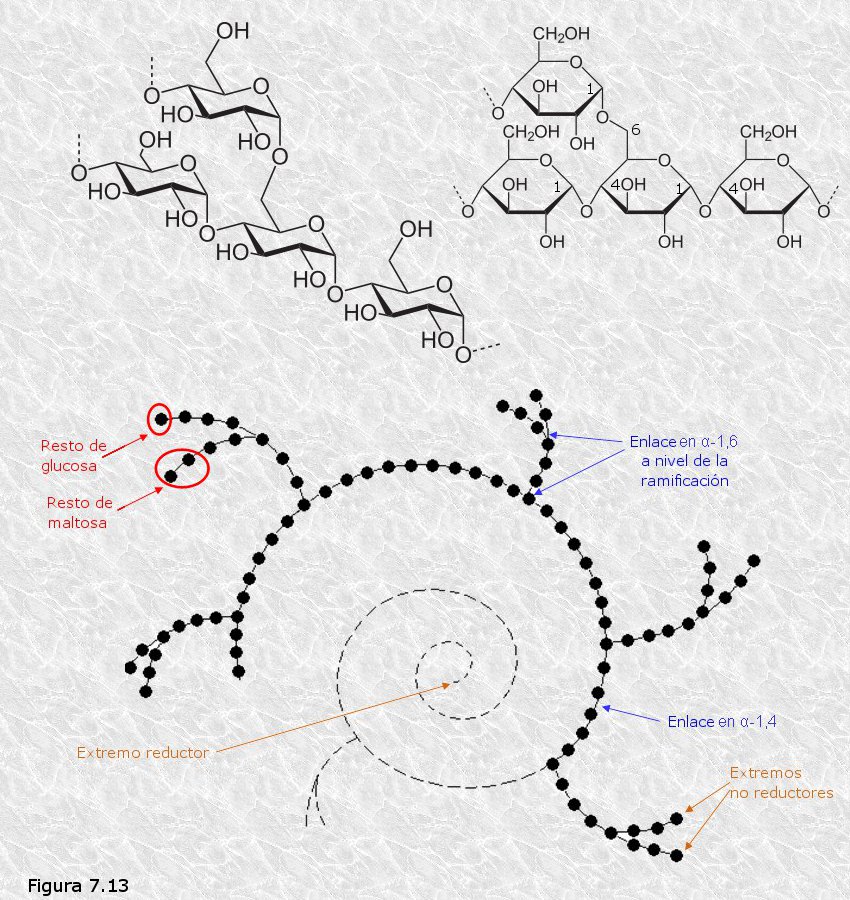
El almidón actúa como sustancia de reserva en las células vegetales. Una parte sustancial de los glúcidos producidos en la fotosíntesis se almacenan en forma de almidón, dando lugar a unos agregados insolubles de gran tamaño, los granos de almidón, que se encuentran en todas las células vegetales, siendo especialmente abundantes en las de las semillas, frutos y tubérculos.
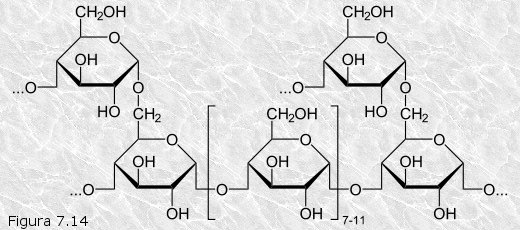 B) Glucógeno.-
Es un polisacárido con estructura muy similar a la de la
amilopectina . Al igual que ésta, está formado por moléculas de
α-D-glucosa unidas por enlaces glucosídicos α(1—›4)
a lo largo de las cadenas, y con puntos de ramificación consistentes
en enlaces α(1—›6)(Figura
7.14).
La diferencia con respecto a la amilopectina estriba en que las
ramificaciones se encuentran menos espaciadas, concretamente cada
8 a 12 restos de glucosa. Esta mayor proximidad entre los
puntos de ramificación hace que el glucógeno sea mucho más compacto
que el almidón, pudiendo alcanzar pesos moleculares del orden de
varios millones de daltons.
Las moléculas de glucógeno presentan un núcleo de naturaleza
proteica consistente en una molécula de glucogenina, una
proteína enzimática que cataliza la unión glucosídica de las
primeras moléculas de glucosa, que quedan covalentemente ancladas a
la propia proteína formando un núcleo alrededor del cual van
creciendo y ramificándose las cadenas del glucógeno mediante la
acción del enzima glucógeno sintetasa (Figura 7.15).
B) Glucógeno.-
Es un polisacárido con estructura muy similar a la de la
amilopectina . Al igual que ésta, está formado por moléculas de
α-D-glucosa unidas por enlaces glucosídicos α(1—›4)
a lo largo de las cadenas, y con puntos de ramificación consistentes
en enlaces α(1—›6)(Figura
7.14).
La diferencia con respecto a la amilopectina estriba en que las
ramificaciones se encuentran menos espaciadas, concretamente cada
8 a 12 restos de glucosa. Esta mayor proximidad entre los
puntos de ramificación hace que el glucógeno sea mucho más compacto
que el almidón, pudiendo alcanzar pesos moleculares del orden de
varios millones de daltons.
Las moléculas de glucógeno presentan un núcleo de naturaleza
proteica consistente en una molécula de glucogenina, una
proteína enzimática que cataliza la unión glucosídica de las
primeras moléculas de glucosa, que quedan covalentemente ancladas a
la propia proteína formando un núcleo alrededor del cual van
creciendo y ramificándose las cadenas del glucógeno mediante la
acción del enzima glucógeno sintetasa (Figura 7.15).
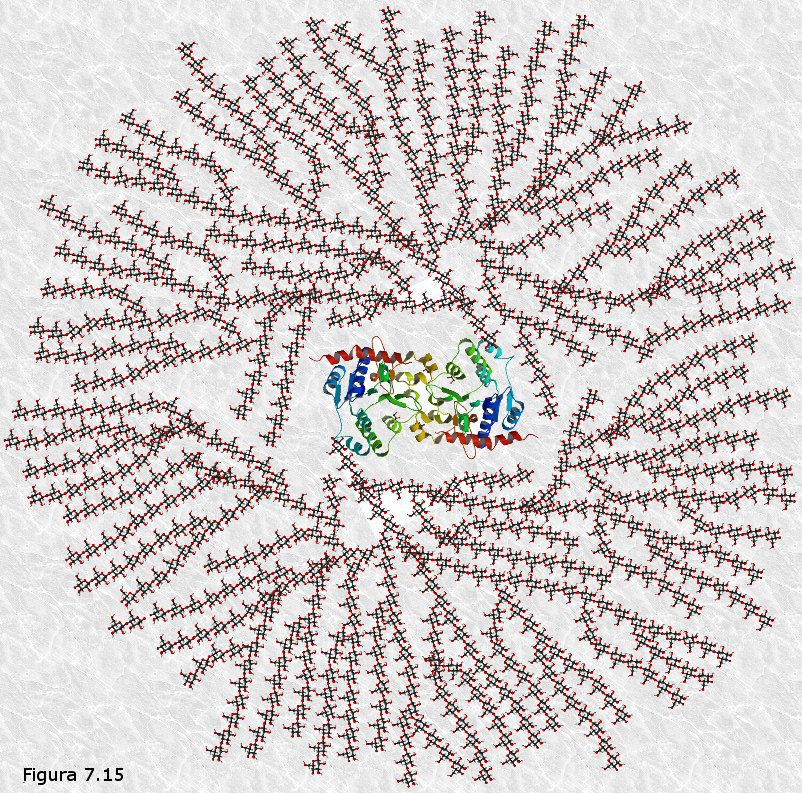
El glucógeno actúa como sustancia de reserva en las células animales. Es especialmente abundante en el hígado, donde puede llegar a representar el 7% de su peso; también abunda en el músculo esquelético. En el interior de las células el glucógeno se encuentra almacenado en forma de gránulos insolubles de gran tamaño.
Cuando las células recurren a sus reservas de almidón o de glucógeno, determinados enzimas van liberando una a una moléculas de glucosa, en forma de derivados fosforilados, las cuales pueden después ser utilizadas como combustible metabólico. La naturaleza ramificada de ambos polisacáridos favorece el que estos enzimas degradativos puedan actuar simultáneamente en muchas ramas aumentando así la velocidad de liberación de glucosa, lo que resulta de gran utilidad para las células cuando necesitan un aporte energético importante de una manera inmediata. Cada molécula de almidón o de glucógeno posee tantos extremos no reductores como ramas y un solo extremo reductor, lo que explica que estos polisacáridos carezcan de poder reductor. Los enzimas degradativos actúan a partir de los extremos no reductores.
Los polisacáridos, dada la gran rapidez con que pueden ser movilizados, constituyen una excelente forma de almacenar energía metabólica a corto plazo. Puede resultar sorprendente que las células almacenen su combustible energético en forma de polisacáridos cuando podrían hacerlo en forma de glucosa libre evitándose así el trabajo químico de sintetizarlos y degradarlos. La razón de que ello sea así estriba en que los polisacáridos se almacenan en forma esencialmente insoluble, contribuyendo muy poco a la presión osmótica del citoplasma. Una cantidad equivalente de glucosa disuelta generaría una presión osmótica muy elevada que podría ser peligrosa para la célula.
Tanto el almidón como el glucógeno pueden ser degradados en el aparato digestivo de los animales por la acción de unos enzimas llamados amilasas. Las amilasas liberan moléculas de glucosa que pueden posteriormente ser absorbidas.
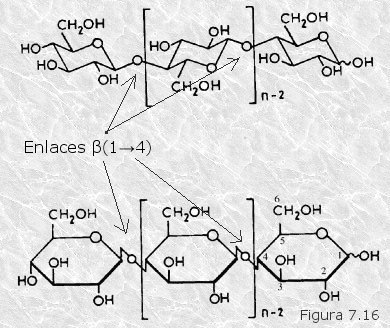 C)
Celulosa.-
Es un polímero lineal (no ramificado) formado por moléculas
de β-D-glucosa unidas mediante enlaces glucosídicos β(1—›4)
(Figura
7.16). Cada cadena de celulosa contiene entre 10.000 y 15.000
restos de glucosa. Estas cadenas, debido a la configuración β de sus
enlaces glucosídicos, adoptan conformaciones muy extendidas que
favorecen la formación de
puentes de hidrógeno entre los grupos hidroxilo de los distintos
restos de glucosa de una misma cadena o de cadenas vecinas
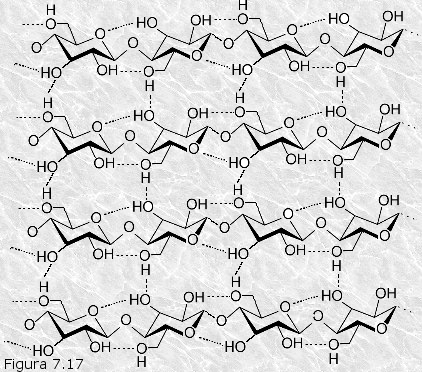
(Figura 7.17). De este
modo se forman fibras supramoleculares que contienen muchas cadenas
individuales de celulosa en disposición paralela e íntimamente
unidas entre sí por puentes de hidrógeno. Tal estructura es la que
confiere a la celulosa su insolubilidad en agua y su resistencia
mecánica características, propiedades estas que la hacen idónea para
desempeñar en las células una función de carácter estructural. La
celulosa es el principal componente de las paredes celulares
vegetales, las cuales proporcionan a las células de las plantas
y
C)
Celulosa.-
Es un polímero lineal (no ramificado) formado por moléculas
de β-D-glucosa unidas mediante enlaces glucosídicos β(1—›4)
(Figura
7.16). Cada cadena de celulosa contiene entre 10.000 y 15.000
restos de glucosa. Estas cadenas, debido a la configuración β de sus
enlaces glucosídicos, adoptan conformaciones muy extendidas que
favorecen la formación de
puentes de hidrógeno entre los grupos hidroxilo de los distintos
restos de glucosa de una misma cadena o de cadenas vecinas
(Figura 7.17). De este
modo se forman fibras supramoleculares que contienen muchas cadenas
individuales de celulosa en disposición paralela e íntimamente
unidas entre sí por puentes de hidrógeno. Tal estructura es la que
confiere a la celulosa su insolubilidad en agua y su resistencia
mecánica características, propiedades estas que la hacen idónea para
desempeñar en las células una función de carácter estructural. La
celulosa es el principal componente de las paredes celulares
vegetales, las cuales proporcionan a las células de las plantas
y
 las algas sostén mecánico y protección frente a los fenómenos
osmóticos desfavorables. Una gran parte de la masa de la madera es
celulosa.
las algas sostén mecánico y protección frente a los fenómenos
osmóticos desfavorables. Una gran parte de la masa de la madera es
celulosa.
Las amilasas que degradan el almidón y el glucógeno no pueden romper los enlaces β glucosídico de la celulosa. El intestino humano (y el de la mayoría de los animales) carece de enzimas que puedan romper este tipo de enlace, por lo que este polisacárido tiene para el hombre un valor alimenticio prácticamente nulo. Este hecho está compensado con creces por la capacidad de la celulosa para generar una gran cantidad de residuos que a su paso limpian y facilitan el buen funcionamiento del aparato digestivo. Algunos animales como las termitas o los rumiantes viven en simbiosis con determinados microorganismos poseedores de enzimas específicos, llamados celulasas, que sí son capaces de degradar la celulosa, por lo que estos animales pueden aprovechar su valor nutritivo.
Además de los descritos, existen en la naturaleza otros homopolisacáridos, algunos de ellos formados por monosacáridos diferentes de la glucosa, como los fructanos, mananos y arabinanos. También hay homopolisacáridos formados por derivados de la glucosa, como la quitina, un polímero de la N-acetil-glucosamina, que es el componente principal del exoesqueleto de los artrópodos.
Entre los heteropolisacáridos los más importantes son los que están formados por dos tipos de unidades monosacarídicas que se alternan a lo largo de sus cadenas. Algunos de ellos son el ácido hialurónico, que se encuentra en el tejido conjuntivo de los animales ejerciendo un papel lubricante, la hemicelulosa, que forma parte de la pared celular vegetal, y la heparina, con notables propiedades anticoagulantes; todos ellos están formados por derivados complejos de la glucosa.
9.-HETERÓSIDOS.
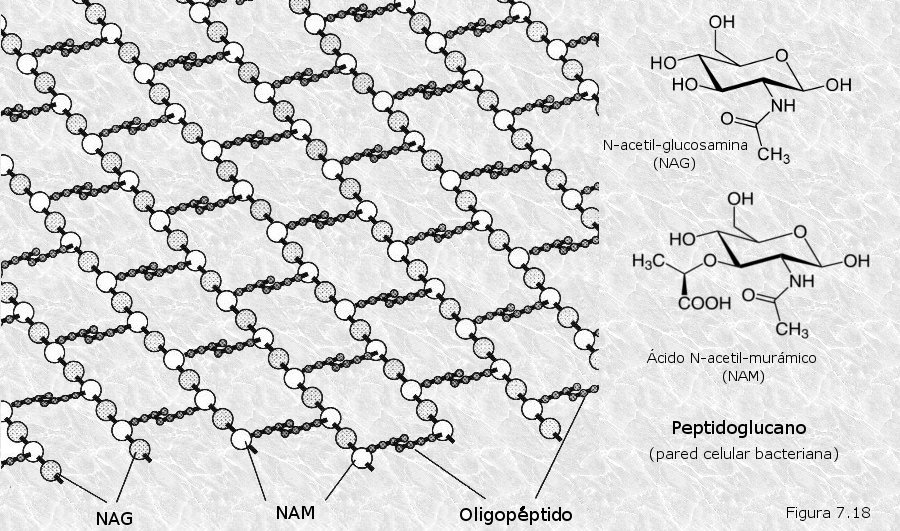
Como se dijo anteriormente, están formados por monosacáridos y otros componentes de naturaleza no azucarada. Ente ellos cabe citar a los glucolípidos, y a las glucoproteínas, que son asociaciones covalentes de cadenas oligosacarídicas con lípidos y proteínas respectivamente; los glucolípidos y glucoproteínas están presentes en muchos lugares de la célula, sobre todo en la cara externa de la membrana plasmática. Un tipo especial de heterósido es el peptidoglucano, componente esencial de las paredes celulares bacterianas, que está constituido por cadenas paralelas de un heteropolisacárido en el que se alternan unidades de N-acetil-glucosamina y de ácido N-acetil-murámico (dos derivados de la glucosa) unidas transversalmente por cadenas de aminoácidos unidos mediante enlaces peptídicos (Figura 7.18).
10.-FUNCIONES DE LOS GLÚCIDOS.
Los glúcidos desempeñan con carácter general en los seres vivos dos tipos de funciones: energéticas y estructurales.
1) Función energética.- La oxidación de los glúcidos libera energía que las células pueden utilizar para realizar sus funciones. La glucosa es el azúcar que con más frecuencia utilizan las células como combustible metabólico primario. Por otra parte, algunos polisacáridos actúan como material de reserva energética que puede ser rápidamente movilizado cuando es necesario. Una ventaja que poseen los glúcidos sobre otras biomoléculas como material energético es que, dada la solubilidad en agua de muchos de ellos, pueden ser transportados muy rápidamente en medio acuoso allí donde resultan necesarios.
2) Función estructural.- Algunos polisacáridos como la celulosa o la quitina presentan propiedades que los hacen idóneos para formar parte de estructuras que deben ofrecer una gran resistencia mecánica, como las paredes celulares vegetales o el exoesqueleto de los artrópodos.
Aunque tradicionalmente se consideraba a los glúcidos como componentes "pasivos" de la maquinaria celular, destinados a servir de combustible metabólico o a formar parte de estructuras más o menos permanentes de las células, en los últimos años se está percibiendo cada vez con mayor claridad que algunos de ellos pueden jugar otros papeles de extraordinaria importancia biológica, como la determinación de la estructura tridimensional de algunas proteínas, los procesos de reconocimiento de señales extracelulares o la acción de los anticuerpos.